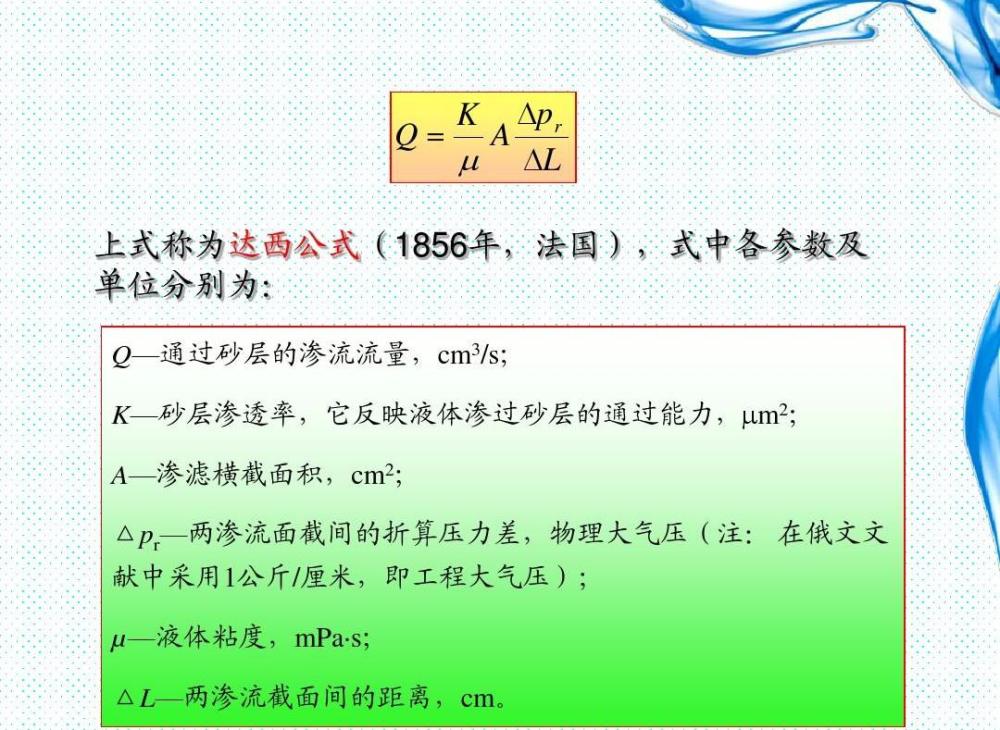
基本原理
液态水的密度幾乎不随壓力升高而改變。但是如果将水的溫度和壓力升高到臨界點Tc=374.3℃,Pc=22.1MPa以上,水的性質發生了極大變化,其密度、介電常數、黏度、擴散系數、熱導率和溶解性等都不同于普通水。
通過測定水在亞臨界到超臨界區的介電常數、離子解離常數及Raman光譜可探索水的溶劑性質和分子結構。結果表明水的定态介電常數從常溫的80變到臨界點的5-10,在450℃或更高時降到2左右。離子解離常數從室溫的10到近臨界區的10,而在超臨界區變成10。水的Raman光譜結果也表明在超臨界狀态下水中隻剩下少部分氫鍵。
這些結果意味着水的行為與非極性壓縮氣體相近,其溶劑性質與低極性有機物相似。因而,碳氫化合物在超臨界水中通常有很高的溶解度。例如,在25℃時,苯在水中的溶解度為0.07%,295℃時上升為35%,在300℃時即超越苯一水混合物的臨界點,隻存在一個相,因此,任何比例的組分都是互溶的。同理,在375℃以上,超臨界水可與氧氣、空氣和氮氣及有機物以任意比例互溶。
與有機物的高溶解度相比,無機鹽在超臨界水中的溶解度非常低,并且随水的介電常數減小而減小,當溫度大于475℃時,無機物在超臨界水中的溶解度急劇減小,呈鹽類析出或以濃縮鹽水的形式存在。如NaCl在300℃水中的溶解度為37%,而在550℃和25MPa的水中的溶解度為120mgL,其原因主要是由水的低介電常數和離子解離常數造成的。
同時,在超臨界水中溶解的無機鹽溶質具有不同于常溫常壓下的特殊性,對于等壓條件下的溫度上升,水的介電常數會降低,有利于溶質的締合;相反,等溫條件下壓力的上升有利于溶質的分解。在高溫低壓的超臨界條件下,當水的介電常數小于15時,水中溶解的溶質會發生大規模的締合作用,即常溫常壓下的強電解質在高溫低壓的超臨界條件下會變為弱電解質,而室溫下的弱電解質則形成中性的締合的配合物。
在氧化過程中,有機污染物中的C,H元素最後轉化成二氧化碳和水;N、S、P和鹵素等雜原子氧化生成氣體、含氧酸或鹽;在超臨界水中鹽類以濃縮鹽水溶液的形式存在或形成固體顆粒而析出,超臨界流體中的水經過冷卻後成為清潔水。因而,超臨界水氧化技術是在不産生有害副産物情況下徹底有效降解有機污染物的一種新方法。
從理論上講,SCWO技術适用于處理任何含有機污染物的廢物,高濃度的有機廢液、有機蒸汽、有機固體、有機廢水、污泥、懸浮有機溶液或吸附了有機物的無機物;廢水中的有機物和氧化劑02,H202在單一相中反應生成CO2和H2O。
出現在有機物中的雜原子氯、硫和磷分别被轉化為HCl、H2SO4和H3PO4,有機氮主要形成N2;在超臨界水的氧化環境不産生N2O。因此SCWO過程無需尾氣處理,不會造成二次污染。另外,當廢水中的有機物濃度大于2%時,可利用反應放出的熱維持過程的熱平衡,從而實現自熱反應。
化學方程式
有機廢物在超臨界水中進行的氧化反應,概括地可以用以下化學方程式表示:
有機化合物+氧化劑(02,H202)→CO2+H20;
有機化合物中的雜原子酸、鹽、氧化物;
酸十NaOH→無機鹽。
相關研究
超臨界逆向蒸發過程,是利用超臨界流體的特性開發的制備脂質體的新方法,SCRPE過程在制備低水溶性藥物脂質體具有獨特的優勢,不僅可以避免大量使用有機溶劑,消除對環境的危害,還可以通過調整體系的壓力和溫度來改變體系的密度(溶劑溶解能力),從而為脂質體的制備及分離處理提供良好的可調性介質,該方法是脂質體技術的一個突破,極大地擴展了超臨界CO_2的應用領域。