簡介
铵離子的性質和鉀離子相近,在溶液中呈+1價。铵鹽都呈白色晶體,加堿研磨(相當于加熱)能生成有刺激性氣味的氨氣(化學式:NH₃),铵鹽受熱會分解。
還原性
铵根離子有較強的還原性(熱力學上),但受動力學因素阻礙,酸性溶液中铵的還原性很多時候難以體現:
例如,強氧化性的氯氣和溴都不會氧化铵:
Br2+2NH4Cl→NH4ClBr2
3Cl2+NH4+—(pH<4.4)→3Cl-+NCl3+4H+
(pH>8.5生成NH2Cl,pH=4.5-5生成NHCl2)
(氯胺,二氯胺,三氯化氮中氯氧化數均為+1)
但也可以在一些反應中或固态物質中體現:
與亞硝酸根反應:
NO2-+NH4+→N2↑+2H2O
硝酸铵爆炸:
NH4NO3—(190℃—200℃慢慢加熱)→N2O↑+2H2O
2NH4NO3—(低溫慢慢加熱)→N2↑+2NO+2H2O
5NH4NO3—(190℃)→2N2↑+4HNO3+9H2O
與氧氣反應:
2O2+NH4+—(硝化細菌)→NO3-+H2O+2H+
重鉻酸铵分解:
(NH4)2Cr2O7—(加熱)→Cr2O3+N2↑+4H2O
高錳酸铵在水中分解:
2MnO4-+2NH4+=2MnO2+N2↑+4H2O
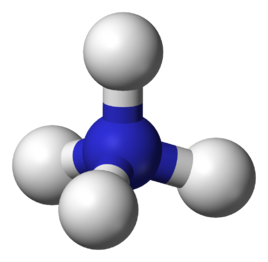
結構
铵離子是正四面體型的,與甲烷互為等電子體。
用途
用于铵鹽中含氮,鹽可用作氮肥,稱為铵态氮肥。此類肥料不宜與堿性肥料混用,否則铵離子會被反應掉從而肥效降低。
常見的铵态氮肥有:硫铵、碳铵、硝铵。
檢驗方法
铵鹽的檢驗方法通常是與堿混合(必要時加熱),會放出氨氣。例如:
NH4HCO3+Ca(OH)2→CaCO3+2H2O+NH3↑
(NH4)2SO4+2NaOH→Na2SO4+2H2O+2NH3↑
原理是铵鹽與堿發生複分解反應,生成新鹽和一水合氨,一水合氨易揮發為氨氣和水。
NH4++OH-=(加熱)→NH3↑+H2O
铵鹽可以與奈斯勒試劑反應生成黃棕色沉澱,用于定性檢驗。
NH4++ 2[HgI4]2- + 4OH- → HgO·Hg(NH2)I + 7I-+ 3H2O
衍生物
铵離子的氫原子可以被其他其他原子或原子團取代形成一個取代铵離子。根據其他其他原子或原子團的數目,铵陽離子被稱為一級、二級、三級或四級。
除季铵陽離子外,有機铵陽離子均為弱酸。
一個形成铵離子的例子:(CH3)2NH和酸形成陽離子:(CH3)2NH2+:
(CH3)2NH+H+→(CH3)2NH2+