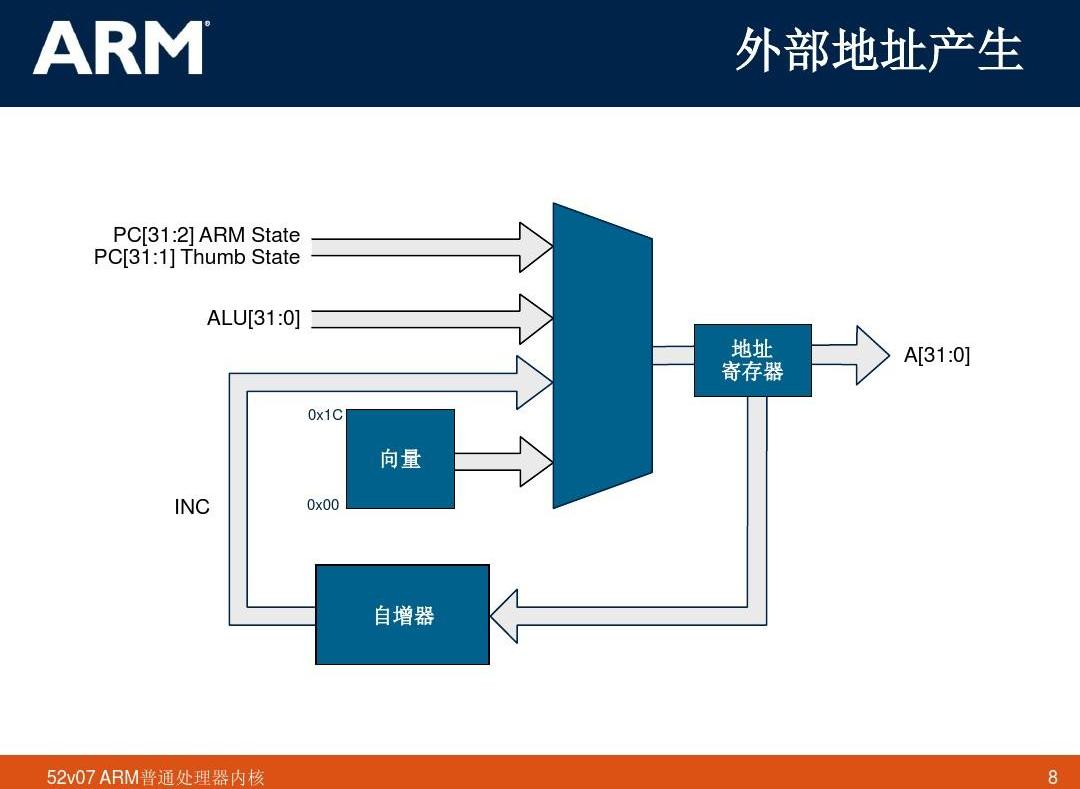
物理性質
1.純硝酸為無色、有刺激性氣味的液體。硝酸溶液為無色液體;濃HNO3中因溶有HNO3分解産生的NO2而呈黃色。
2.硝酸沸點低、易揮發,在空氣中遇水蒸氣而産生白霧。
3.通常使用的硝酸為69%的硝酸,發煙硝酸為硝酸含量約為86%~97.5%
化學性質
1、強酸性:硝酸是一元強酸,具有酸的通性。
2、不穩定性
注意:濃度越大,越易分解;
硝酸應保存在玻璃塞(HNO3腐蝕橡膠)棕色細口瓶中,放于陰涼處。
3、強氧化性:
與金屬反應:除Pt、Au外的金屬均能與HNO3反應。
注意:常溫下,濃HNO3使Fe、Al等金屬鈍化;
金屬與硝酸反應不産生H2。
與非金屬反應:能氧化C、S、P等非金屬。
與H2S、HBr、HI、SO2、KI、Na2SO3等物質反應。
說明:氧化性:濃硝酸>稀硝酸;
王水:濃硝酸和濃鹽酸按體積比1:3混合而成。王水有很強的氧化性,能溶解Pt、Au等金屬。
(注:一般我們認為濃稀之間的界線是6mol/L。這個隻是一般的,不能說大于6mol/L的硝酸和銅反應生成NO2,不到6mol/L的硝酸和銅反應生成NO。)
鑒别稀硝酸和濃硝酸
1、在冷的硝酸中加入鐵或鋁,若無明顯現象,則是濃硝酸,若鐵或鋁的表面産生氣泡則是稀硝酸。
2、直接看,冒白霧的是濃硝酸,沒有白霧的是稀硝酸,這裡是利用硝酸的揮發性。