物理性質
性狀:無色結晶
密度:3.988g/cm3。
熔點:645℃
沸點:1290℃,
溶解性:極易溶于水[100克H2O中162克(0℃),259克(90℃)]。微溶于甲醇、乙醇,不溶于丙酮。在空氣中吸濕潮解。
晶格能:659kJ/mol。
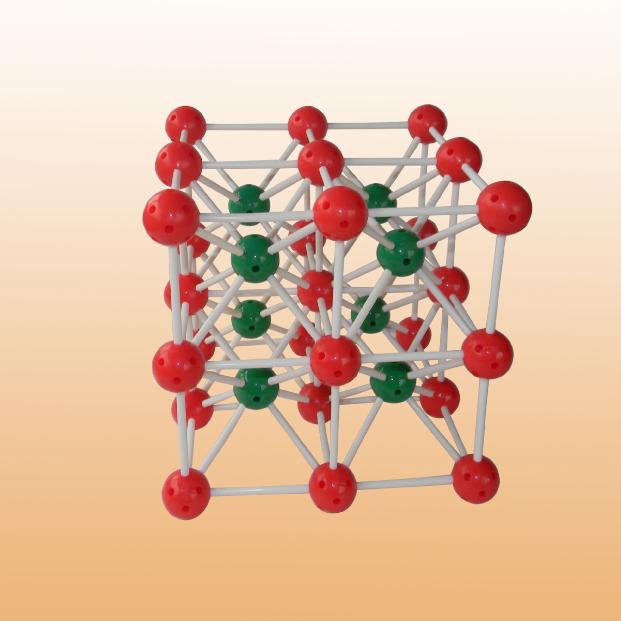
結構
低于445℃,氯化铯晶胞是素晶胞(可看成氯離子作簡單立方堆積,铯離子填充立方空隙)。采取這種晶體結構的化合物包括CsCl,CsBr,CsI,TlCl,TlBr和NH4Cl等。高于445℃,氯化铯也具有配位數8的面心立方結構[見三師大合編,潘道皚等編《物質結構》第二版,高教社,1989:545]。
用途
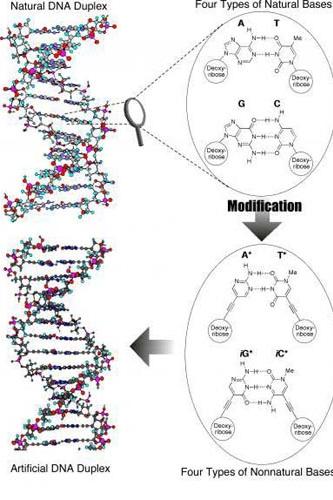
點滴分析三價鉻和镓。無線電、電視機真空管最後的抽成真空。X射線熒光屏。無線電反襯介質。制造铯。氣相色譜固定液(最高使用溫度450℃,溶劑為水),用于高溫色譜分析二聯苯、三聯苯。用于顯微鏡分析,密度梯度離心。制取金屬铯和含铯單晶的原料;分析試劑;用于制備導電玻璃;用于通過密度梯度離心方法制備從DNA中分離RNA的溶液。
合成方法
1、将碳酸铯溶解于少量水中。在不斷攪拌下慢慢加入相對密度為1.18的鹽酸,加熱反應:
Cs2CO3+2HCl→2CsCl+2H2O+CO2
當pH=3時,煮沸半小時加入氫氧化铯使溶液pH值到中性。過濾,濾液蒸發濃縮至大量結晶析出,冷至室溫,分離母液,潔淨與100ºC烘幹,即為成品。
2、用碳酸铯溶于鹽酸,再濃縮其溶液以制取氯化铯。通常可得到純度為99.5%的氯化铯,可直接使用。對不夠純淨的氯化铯,可采用下列方法精制。
将15g的氯化铯,加熱溶于100mL的水中。将化學計量24.2g氯化汞溶于25mL4mol的鹽酸中。趁熱将此HgCl2/HCl溶液加到上述溶液中,攪拌混合,冷卻,即可析出CsHgCl3結晶。吸濾,收集結晶,棄去母液。将結晶溶于120mL的熱水中,冷卻後再次有結晶析出。為此反複進行2~3次重結晶,堿金屬可降至0.01%以下,最後将結晶溶于熱水,通入H2S氣體使溶液達到飽和,就有HgS沉澱析出,濾去HgS,收集濾液,蒸發至幹,即可得純淨的氯化铯。
貯藏運輸
庫房低溫通風幹燥。
安全術語
S36/37Wearsuitableprotectiveclothingandgloves.
穿戴适當的防護服和手套。
風險術語
R68Possibleriskofirreversibleeffects.
可能有不可逆後果的危險。有毒物質
計算化學數據
1、疏水參數計算參考值(XlogP):無
2、氫鍵供體數量:0
3、氫鍵受體數量:1
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積:0
7、重原子數量:2
8、表面電荷:0
9、複雜度:2
10、同位素原子數量:0
11、确定原子立構中心數量:0
12、不确定原子立構中心數量:0
13、确定化學鍵立構中心數量:0
14、不确定化學鍵立構中心數量:0
15、共價鍵單元數量:2