操作步骤
装置选择
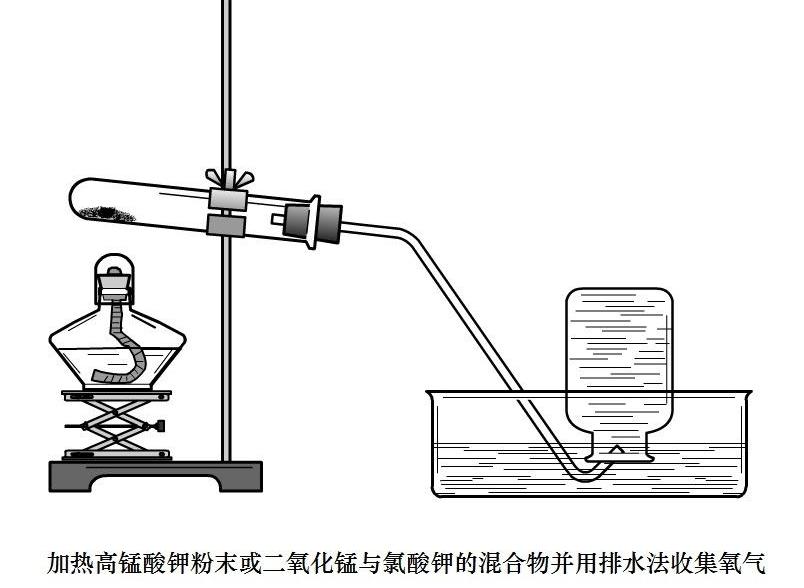
1.用高锰酸钾或氯酸钾制氧气选甲装置:固体与固体加热制气体(实验室常用说法:固固加热型);
2.用过氧化氢制氧气选乙装置:液体与固体不加热制气体(实验室常用说法:固液常温型)。
方法步骤
高锰酸钾制取氧气
步骤:查—装—定—点—收—移—熄;
查——检查装置的气密性;
装——装药品;
定——把试管固定到铁架台上;
点——点燃酒精灯加热(先预热,注意:一律先让试管均匀受热,否则会因冷热不均炸裂试管);
收——收集气体(可以使用排水法、向上排空气法);
移——把导管从水槽中取出(如果使用向上排空气法,此步骤基本不需要,但是最好先取出导管在盖上玻片);
熄——熄灭酒精灯。
注意点:
①试管口略向下倾斜:防止冷凝水倒流回试管底部炸裂试管;
②药品平铺在试管的底部:先预热,之后可以将酒精灯的外焰对准装有药品部位定向加热;
③铁夹夹在离管口约1/3处;
④导管应稍露出橡皮塞:便于气体排出(大约0.5cm);
⑤试管口应放一团棉花:防止高锰酸钾粉末进入导管并堵塞导管,使所制得气体无法较好排出;
⑥排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气,此时收集气体不纯);
⑦实验结束时,先移走导管,再熄灭酒精灯:防止水槽中的冷水倒吸进热的试管引起试管炸裂;
⑧用向上排空气法收集气体时,导管伸到集气瓶底部:以便把空气排尽。
过氧化氢(双氧水)制氧气
步骤:查——装——收;
查——检查装置的气密性:用夹子把导管夹上(应使用两节导管,中间用较短橡皮管连接,便于检查),然后往长颈漏斗中加水,长颈漏斗的颈部中的水柱如不下降,说明气密性良好;
装——装药品,先装固体,后装液体(防止液体飞溅);
收——收集气体(同上高锰酸钾收集法)。
注意点:
①长颈漏斗的颈部应在液面以下(液封):防止气体从长颈漏斗泄露,可用分液漏斗代替(可控制反应速率);
②导管应稍露出橡皮塞:便于气体排出。
氧气检验
检验方法:
检验:用带火星的木条伸入集气瓶内,如果木条复燃,证明是O2。
验满:用带火星的木条放在集气瓶瓶口,如果木条复燃,证明O2已满。
排水法:
当集气瓶瓶口冒气泡时(刚开始排出的是试管中的空气,等气泡连续均匀冒出时,才是纯氧);
实验室制取氧气是初级化学的一个实验,通常二氧化锰是催化剂,实验完毕后,可以用过滤法回收。
向上排气法(O2密度大于空气)。
文字表达
实验室制取氧气方法主要有三种,其文字表达式如下:
高锰酸钾————→锰酸钾+二氧化锰+氧气(加热)
氯酸钾————→氯化钾+氧气(二氧化锰做催化剂)
过氧化氢+二氧化锰—→水+氧气(二氧化锰做催化剂、加热)
制氧口诀
二氧化锰氯酸钾;混和均匀把热加。
制氧装置有特点;底高口低略倾斜。
二氧化锰
二氧化锰MnO2
一种两性氧化物.它是一种常温下非常稳定的黑色或棕色粉末状固体为软锰矿的主要成分,密度5.0g/cm3不溶于水,是最重要的一种锰的氧化物。氧化锰粉尘可引起人的锰尘肺。高价锰氧化物,不论侵入机体的途径,其毒性作用对大脑有损伤。
遇还原剂时,表现为氧化性。如将二氧化锰放到氢气流中加热至1400K得到一氧化锰;将二氧化锰放在氨气流中加热,得到棕黑色的三氧化二锰;将二氧化锰跟浓盐酸反应,则得到二氯化锰和氯气。
遇强氧化剂时,还表现为还原性。如将二氧化锰,碳酸钾和硝酸钾或氯酸钾混合熔融,可得到暗绿色熔体,将熔体溶于水冷却可得六价锰的化合物锰酸钾。在酸件介质中是一种强氧化剂。
大量用于炼钢,并用于制玻璃,陶瓷,搪瓷,干电池以及用作催化剂等。
二氧化锰也被用作颜料、有色玻璃等。